Формула гексафторид серы – Фторид серы(VI) • Справочник структурных формул • Кировская Молекулярная Биология
Гексафторид серы: что это такое?
В последнее время вырос интерес к такому химическому веществу, как гексафторид серы. Этому способствовали развлекательные передачи на телевидении, среди которых наиболее известны «Хорошие шутки» и «Разрушители мифов». Особенно заинтересовал многих тот факт, что с помощью этого вещества можно менять тембр голоса – он становится очень низким. Люди решили, что это прекрасная идея для вечеринок, конкурсов и прочего досуга. Если есть спрос, будут и предложения: в интернете нетрудно найти объявления о продаже гексафторида серы. Но, прежде чем кидаться покупать это вещество, нелишним будет разобраться, что оно собой представляет и насколько безопасно для человека.
 Гексафторид серы, он же – SF6, он же – шестифтористая сера, он же – элегаз, — неорганическое химическое соединение. Известно оно уже более 100 лет и примерно столько же успешно используется человеком в своих целях. Химические свойства: инертный, нетоксичный, тяжёлый газ (в 5 раз тяжелее воздуха). Вещество абсолютно бесцветно, обладает высокой электрической прочностью и высоким пробивным напряжением. Возможны два пути его образования – из простых веществ и при разложении сложных фторидов серы. Благодаря своим физико-химическим свойствам используется как диэлектрик в электротехнической промышленности, как технологическая среда — в электронной промышленности, а также как инертная среда для получения сплавов — в металлургии. В последнее время элегаз (сокращение от «электрический газ») применяется при тушении пожаров как огнетушащее средство. Это основные сферы применения гексафторида серы.
Гексафторид серы, он же – SF6, он же – шестифтористая сера, он же – элегаз, — неорганическое химическое соединение. Известно оно уже более 100 лет и примерно столько же успешно используется человеком в своих целях. Химические свойства: инертный, нетоксичный, тяжёлый газ (в 5 раз тяжелее воздуха). Вещество абсолютно бесцветно, обладает высокой электрической прочностью и высоким пробивным напряжением. Возможны два пути его образования – из простых веществ и при разложении сложных фторидов серы. Благодаря своим физико-химическим свойствам используется как диэлектрик в электротехнической промышленности, как технологическая среда — в электронной промышленности, а также как инертная среда для получения сплавов — в металлургии. В последнее время элегаз (сокращение от «электрический газ») применяется при тушении пожаров как огнетушащее средство. Это основные сферы применения гексафторида серы.
Но развлекательное телевидение расширило область применения этого вещества и популяризировало его. Причиной этому послужила его способность изменять человеческий голос: если вдохнуть гексафторид серы, голос станет чудовищно, неестественно низким. Интересно, почему такое происходит? Нередко можно встретить мнение, что элегаз действует на голосовые связки, вызывает их кратковременный отёк и таким образом «понижает» голос. Это совсем не так. Дело в том, что сами по себе голосовые связки не образуют громкого звука. Речевой аппарат человека помимо связок включает в себя ещё и резонаторы. Один из таких резонаторов – глотка. На тембр голоса влияет, прежде всего, среда этого резонатора. Если эта среда – воздух, то мы слышим обыкновенный, привычный всем голос. Но стоит изменить среду, и мы услышим другой, совершенно чужой голос. Объясняется это следующим принципом: чем легче газ и быстрее движение его молекул, тем выше будет голос. И наоборот: чем тяжелее газ, тем медленнее движение молекул, тем ниже тембр. Гелий легче воздуха, поэтому при вдыхании этого газа голос становится писклявым, очень тонким. Гексафторид серы, как уже говорилось, в 5 раз тяжелее, и если вдохнуть его, голос станет грубым и низким. Вот и всё: такой забавный эффект элегаза объяснятся кратковременным изменением среды резонатора. Вдыхание этого вещества не способно нанести вреда организму, если оно не содержит посторонних примесей.
Если вы захотите приобрести гексафторид серы, цена не должна быть для вас определяющей. Никто не спорит, что и это немаловажно, но здоровье дороже. Поэтому приобретая элегаз, поинтересуйтесь у продавца, «чистый» ли это гексафторид, не содержит ли каких-либо других добавок. Это обезопасит вас и ваших гостей, которых вы соберётесь развлекать элегазом, от неожиданных и неприятных сюрпризов.
fb.ru
Гексафторид серы Википедия
| Фторид серы | |
|---|---|
 | |
| Общие | |
| Традиционные названия | гексафторид серы, шестифтористая сера, элегаз |
| Хим. формула | SF6 |
| Физические свойства | |
| Состояние | газ |
| Молярная масса | 146,06 г/моль |
| Плотность | Газ: 6,164 г/л Жидкость: 1,33 г/см³ |
| Энергия ионизации | 19,3 ± 0,1 эВ[1] |
| Термические свойства | |
| Т. плав. | −50,8 °C |
| −83 ± 1 градус Фаренгейта[1] | |
| Т. кип. | сублимация при −63,9 °C |
| Мол. теплоёмк. | 97,15 Дж/(моль·К) |
| Теплопроводность | 0,012058 Вт/(м·K) |
| Энтальпия образования | −1219 кДж/моль |
| Давление пара | 21,5 ± 0,1 атм[1] |
| Структура | |
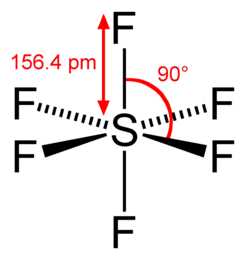
| Координационная геометрия | октаэдрическая |
| Кристаллическая структура | орторомбическая |
| Дипольный момент | 0 Д |
| Классификация | |
| Рег. номер CAS | 2551-62-4 |
| PubChem | 17358 |
| Рег. номер EINECS | 219-854-2 |
| SMILES | |
| InChI | |
| RTECS | WS4900000 |
| ChEBI | 30496 |
| Номер ООН | 1080 |
| ChemSpider | 16425 |
| Безопасность | |
| Токсичность | малотоксичен |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Гексафторид серы (также элегаз или шестифтористая сера, SF6) — неорганическое вещество, при стандартных условиях представляет собой тяжёлый газ (в 5 раз тяжелее воздуха). Соединение было впервые получено и описано в 1900 году Анри Муассаном в ходе работ по изучению химии фтора.
Методы получения
Возможно получать гексафторид серы из простых веществ:
- S+3F2→SF6{\displaystyle {\mathsf {S+3F_{2}\rightarrow SF_{6}}}}
Также гексафторид серы образуется при разложении сложных фторидов серы:
- S2F10→SF6+SF4{\displaystyle {\mathsf {S_{2}F_{10}\rightarrow SF_{6}+SF_{4}}}}
Физико-химические свойства
Практически бесцветный газ, без запаха и вкуса. Обладает высоким пробивным напряжением (89 кВ/см — примерно в 3 раза выше, чем у воздуха при нормальном давлении).
Плохо растворим в воде (1 объём SF6 в 200 объёмах воды), этаноле и диэтиловом эфире
Плотность элегаза при температуре 273 K и давлении 0,1 МПа составляет 6,56 кг/м³. Относительная диэлектрическая проницаемость — 1,0021. Полное число степеней свободы молекулы элегаза равно 21, из них три степени свободы — в поступательном движении, три — во вращательном, а остальные — в колебательном. Диаметр молекулы равен 5,33 Å.
Термодинамические величины
Химические свойства
Гексафторид серы — достаточно инертное соединение, не реагирует с водой, вероятно, из-за кинетических факторов. Не реагирует также с растворами HCl и NaOH[4], однако при действии восстановителей могут протекать некоторые реакции.
В составе молекулы газа 21,95 % серы и 78,05 % фтора по массе.
Взаимодействие с металлическим натрием проходит только при нагревании, однако уже при 64 °C взаимодействует с раствором натрия в аммиаке:
- SF6+8Na→Na2S+6NaF{\displaystyle {\mathsf {SF_{6}+8Na\rightarrow Na_{2}S+6NaF}}}
Гексафторид серы реагирует с литием с выделением большого количества тепла:
- SF6+6Li→S+6LiF{\displaystyle {\mathsf {SF_{6}+6Li\rightarrow S+6LiF}}}
При этом продукты реакции — элементарная сера и фторид лития — имеют меньший объём, чем исходные вещества, что нашло применение в некоторых экзотических тепловых двигателях (см. ниже).
С водородом и кислородом гексафторид не реагирует. Однако, при сильном нагревании (до 400 °C) SF6 взаимодействует с сероводородом, а при 30 °C — с иодоводородом:
- 2SF6+6h3S→S8+12HF{\displaystyle {\mathsf {2SF_{6}+6H_{2}S\rightarrow S_{8}+12HF}}}
- SF6+8HI→6HF+h3S+4I2{\displaystyle {\mathsf {SF_{6}+8HI\rightarrow 6HF+H_{2}S+4I_{2}}}}
При повышенном давлении и температуре около 500 °C SF6 окисляет PF3 до PF5:
- SF6+PF3→PF5+SF4{\displaystyle {\mathsf {SF_{6}+PF_{3}\rightarrow PF_{5}+SF_{4}}}}
Применение
- как изолятор и теплоноситель в высоковольтной электротехнике;
- как технологическая среда в электронной и металлургической промышленности;
- в системах газового пожаротушения в качестве пожаротушащего вещества;
- как хладагент благодаря высокой теплоёмкости, низкой теплопроводности и низкой вязкости[5];
- для улучшения звукоизоляции в стеклопакетах;
- в полупроводниковой промышленности для плазмохимического травления кремния;
- как окислитель в некоторых экзотических тепловых двигателях — например, в паротурбинной установке американской малогабаритной 324-мм противолодочной торпеды Mark 50, где он используется для окисления металлического лития.
При вдыхании наблюдается эффект пониженной тональности голоса, противоположный действию гелия[6].
Применение в электротехнике
Название «элегаз» шестифтористая сера получила от сокращения «электрический газ». Уникальные свойства элегаза были открыты в СССР, его применение также началось в Советском Союзе. В 30-х годах известный учёный Б. М. Гохберг в ЛФТИ исследовал электрические свойства ряда газов и обратил внимание на некоторые свойства шестифтористой серы SF 6 (элегаза)[7]. Потребность в элегазе появилась в стране в начале 1980-х годов и была связана с разработкой и освоением электрооборудования для передач постоянного тока сверхвысокого напряжения. Его промышленное производство в РФ было освоено в 1998 году на Кирово-Чепецком химическом комбинате[8].
Электрическая прочность при атмосферном давлении и зазоре 1 см составляет 89 кВ/см. Характерным является очень большой коэффициент теплового расширения и высокая плотность. Это важно для энергетических установок, в которых проводится охлаждение каких-либо частей устройства, так как при большом коэффициенте теплового расширения легко образуется конвективный поток, уносящий тепло[9].
В центре молекулы элегаза расположен атом серы, а на равном расстоянии от него в вершинах правильного октаэдра располагаются шесть атомов фтора. Это определяет высокую эффективность захвата электронов молекулами, их относительно большую длину свободного пробега и слабую реакционную способность. Поэтому элегаз обладает высокой электрической прочностью.
Элегаз безвреден в смеси с воздухом. Однако вследствие нарушения технологии производства элегаза или его разложения в аппарате под действием электрических разрядов (дугового, коронного, частичных), в элегазе могут возникать чрезвычайно активные в химическом отношении и вредные для человека примеси, а также различные твёрдые соединения, оседающие на стенах конструкции. Интенсивность образования таких примесей зависит от наличия в элегазе примесей кислорода и особенно паров воды.
Некоторое количество элегаза в электротехнической аппаратуре также разлагается в процессе нормальной работы. Например, коммутация тока 31,5 кА в выключателе 110 кВ приводит к разложению 5—7 см³ элегаза на 1 кДж выделяемой в дуге энергии.
Стоимость элегаза довольно высока, однако он нашёл достаточно широкое применение в технике, особенно в высоковольтной электротехнике. Он прежде всего используется как диэлектрик, то есть в качестве основной изоляции для комплектных распределительных устройств, высоковольтных измерительных трансформаторов тока и напряжения и др[10]. Также элегаз используется как среда дугогашения в высоковольтных выключателях[11].
Основные преимущества элегаза перед его основным «конкурентом», трансформаторным маслом, это:
- взрыво- и пожаробезопасность;
- снижения массо-габаритных показателей конструкции за счёт уменьшения изоляционных промежутков и улучшенных условий охлаждения токоведущих частей[источник не указан 1910 дней].
Регламентирующие стандарты
IEC
- IEC 60376:2005 — Технические условия на элегаз (SF6) технического сорта для электрического оборудования.
- IEC 60480:2004 — Руководство по проверке и обработке серы шестифтористой (SF6), взятой из электротехнического оборудования, и технические условия на её повторное использование.
EN[en]
- EN 60376:2005 — Технические условия на элегаз (SF6) технического сорта для электрического оборудования.
- EN 60480:2004 — Руководство по проверке и обработке элегаза (SF6), взятого из электротехнического оборудования, и технические условия на его повторное использование.
Вредное воздействие
- Основной источник: [12]
По степени воздействия на организм человека относится к малоопасным веществам (4-й класс согласно ГОСТ 12.1.007-76).
Имеется возможность отравления продуктами распада элегаза (низшими фторидами), образующимися, например, при работе дугогасительных камер в высоковольтных выключателях.
Потенциал разрушения озонового слоя ODP = 0.
Сильнейший известный парниковый газ, потенциал глобального потепления GWP = 24 900. Из-за небольших объёмов изготовления вклад в глобальное потепление не превышает 0,2 %. Регламентируется Киотским протоколом.
Интересные факты
- Если наполнить гексафторидом серы открытый сверху сосуд (так как газ тяжелее воздуха, то он не будет «выливаться» из сосуда) и поместить туда лёгкую лодочку, сделанную, например, из фольги, то лодочка будет держаться на поверхности и не «утонет». Этот опыт был показан в передаче «Разрушители легенд» как фокус с «прозрачной водой»[13]. Так же, из-за высокой плотности, скорость звука в этом газе значительно ниже, чем в воздухе, что приводит к комичному эффекту при вдыхании газа — голос становится очень низким и грубым, подобно голосу Дарта Вейдера. Опыт также демонстрировался в передаче «Разрушители легенд». Аналогичный эффект создаёт и ксенон. А гелий — который в 6 раз легче воздуха — при вдыхании наоборот создаёт тонкий и писклявый голос.
Примечания
- ↑ 1 2 3 http://www.cdc.gov/niosh/npg/npgd0576.html
- ↑ Свойства гексафторида серы на сайте «Химик.ру»
- ↑ 1 2 Sulfur hexafluoride. Air Liquide Gas Encyclopedia. Проверено 22 февраля 2013.
- ↑ Успехи химии, 1975, Том 44, Номер 2, Страницы 193—213.
- ↑ Применение шестифтористой серы
- ↑ Фрагмент передачи «Разрушители мифов»
- ↑ Гохберг Б. М. Ленинградский физико-технический институт Академии наук СССР (рус.) // Успехи физических наук. — 1940. — Т. XXIV, вып. 1. — С. 11-20. См. стр. 16-17, раздел «Электрическая прочность газов»
- ↑ Уткин В. В. Завод у двуречья. Кирово-Чепецкий химический комбинат имени Б. П. Константинова: строительство, развитие, люди. — Киров: ОАО «Дом печати — Вятка», 2007. — Т. 4 (1973—1992), часть 1. — С. 66—67. — 144 с. — 1000 экз. — ISBN 978-5-85271-293-6.
- ↑ Коробейников С.М., д.ф.м.н., профессор. Диэлектрические материалы. 4.1.2. Электроотрицательные газы, применение газообразных диэлектриков. (рус.). Проверено 2 июня 2011. Архивировано 20 февраля 2012 года.
- ↑ ЗВА :: Измерительные трансформаторы с газовой изоляцией
- ↑ Применение SF6 в высоковольтной электронике.
- ↑ Элегаз. Свойства
- ↑ Выпуск 105. Вирусное видео. 6 сезон
Литература
- Гохберг Б. М. Элегаз — электрическая газовая изоляция (рус.) // «Электричество». — 1947. — № 3. — С. 15.
См. также
wikiredia.ru
Фторид серы(VI) — это… Что такое Фторид серы(VI)?
Гексафторид серы (также элегаз или шестифтористая сера, SF6) — неорганическое вещество, при нормальных условиях тяжёлый газ, в 5 раз тяжелее воздуха. Соединение было впервые получено и описано в 1900 году Анри Муассаном в ходе работ по изучению химии фтора.
Методы получения
Возможно получать гексафторид серы из простых веществ:
Также гексафторид серы образуется при разложении сложных фторидов серы:
Физико-химические свойства
Практически бесцветный газ, обладающий высоким (89 кВ/см) пробивным напряжением. Электрическая прочность элегаза зависит от давления, она в 2-4 раза выше, чем у воздуха.
В нем содержится 21,95 % серы и 78,05 % фтора. При нормальном давлении элегаз может находиться в любом из трёх агрегатных состояний при температуре до минус 50,8 °С.
Плохо растворим в воде (1 объём SF6 в 200 объёмах воды), этиловом спирте и диэтиловом эфире[1], хорошо растворим в нитрометане[2].
Плотность элегаза при T=273 K и давлении р=0,1 МПа составляет 6,56 кг/м³. Относительная диэлектрическая проницаемость — 1,0021. Полное число степеней свободы молекулы элегаза равно 21, из них три степени свободы — в поступательном движении, три — во вращательном, а остальные — в колебательном. Диаметр молекулы равен 5,33 Å.
Термодинамические величины
Химические свойства
Гексафторид серы — достаточно инертное соединение, не реагирует с водой, вероятно из-за кинетических факторов, так как свободная энергия Гиббса реакции существенно отрицательна. Не реагирует также с растворами HCl и NaOH[3], однако при действии восстановителей могут протекать некоторые реакции.
Взаимодействие с металлическим натрием проходит только при нагревании, однако уже при 64 °C взаимодействует с раствором натрия в аммиаке.
С водородом и кислородом гексафторид не реагирует. Однако, при сильном нагревании (до 400 °C) SF6 взаимодействует с сероводородом, а при 30 °C — с иодоводородом:
При повышенном давлении и температуре около 500 °C SF6 окисляет PF3 до PF5:
Применение
- как изолятор и теплоноситель в высоковольтной электротехнике;
- как технологическая среда в электронной и металлургической промышленности;
- в системах газового пожаротушения в качестве пожаротушащего вещества;
- как хладагент благодаря высокой теплоёмкости, низкой теплопроводности и низкой вязкости;[4];
- для изменения тембра голосовых связок (эффект пониженной тональности голоса), противоположно гелию[5];
- для улучшения звукоизоляции в стеклопакетах;
- в полупроводниковой промышленности для плазмохимического травления кремния.
- в термодинамике. При добавлении в состав рабочего тела вертикальной тепловой трубы занимает пространство между жидкостью и паром рабочего тела, снижает парциальное давление паров на жидкость и обеспечивает принудительное удаление паров от поверхности жидкости при температурах ниже температуры кипения; обеспечивает конденсацию паров при повышенных температурах, придавая тепловой трубе свойства самодействующего теплового насоса. Патент Украины № 97882.
Применение в электротехнике
Название «элегаз» шестифтористая сера получила от сокращения «электрический газ». Уникальные свойства элегаза были открыты в СССР, его применение также началось в Советском Союзе. В 30-х годах известный учёный Б. М. Гохберг в ЛФТИ исследовал электрические свойства ряда газов и обратил внимание на некоторые свойства шестифтористой серы SF6 (элегаза)[6]. Электрическая прочность при атмосферном давлении и зазоре 1 см составляет Е=89 кВ/см. Характерным является очень большой коэффициент теплового расширения и высокая плотность. Это важно для энергетических установок, в которых проводится охлаждение каких-либо частей устройства, так как при большом коэффициенте теплового расширения легко образуется конвективный поток, уносящий тепло[7].
В центре молекулы элегаза расположен атом серы, а на равном расстоянии от него в вершинах правильного октаэдра располагаются шесть атомов фтора. Это определяет высокую эффективность захвата электронов молекулами, их относительно большую длину свободного пробега и слабую реакционную способность. Поэтому элегаз обладает высокой электрической прочностью.
Элегаз безвреден в смеси с воздухом. Однако вследствие нарушения технологии производства элегаза или его разложения в аппарате под действием электрических разрядов (дугового, коронного, частичных), в элегазе могут возникать чрезвычайно активные в химическом отношении и вредные для человека примеси, а также различные твёрдые соединения, оседающие на стенах конструкции. Интенсивность образования таких примесей зависит от наличия в элегазе примесей кислорода и особенно паров воды.
Некоторое количество элегаза в электротехнической аппаратуре также разлагается в процессе нормальной работы. Например, коммутация тока 31,5 кА в выключателе 110 кВ приводит к разложению 5-7 см³ элегаза на 1 кДж выделяемой в дуге энергии.
Стоимость элегаза довольно высока, однако он нашёл достаточно широкое применение в технике, особенно в высоковольтной электротехнике. Он прежде всего используется как диэлектрик, то есть в качестве основной изоляции для комплектных распределительных устройств, высоковольтных измерительных трансформаторов тока и напряжения и др.[8] Также элегаз используется как среда дугогашения в высоковольтных выключателях[9].
Основные преимущества элегаза перед его основным «конкурентом», трансформаторным маслом, это:
- взрыво- и пожаробезопасность;
- снижения массо-габаритных показателей конструкции за счёт уменьшения изоляционных промежутков и улучшенных условий охлаждения токоведущих частей.
Регламентирующие стандарты
IEC
- IEC 60376:2005 — Технические условия на элегаз (SF6) технического сорта для электрического оборудования.
- IEC 60480:2004 — Руководство по проверке и обработке серы шестифтористой (SF6), взятой из электротехнического оборудования, и технические условия на ее повторное использование.
EN
- EN 60376:2005 — Технические условия на элегаз (SF6) технического сорта для электрического оборудования.
- EN 60480:2004 — Руководство по проверке и обработке элегаза (SF6), взятого из электротехнического оборудования, и технические условия на его повторное использование.
Вредное воздействие
- Основной источник: [10]
По степени воздействия на организм человека относится к малоопасным веществам (4-й класс согласно ГОСТ 12.1.007-76).
Потенциал разрушения озонового слоя ODP = 0
Потенциал глобального потепления GWP = 24 900 (регламентируется Киотским протоколом).
Интересные факты
- Если наполнить гексафторидом серы открытый сверху сосуд (так как газ тяжелее воздуха, то он не будет «выливаться» из сосуда), и поместить туда лёгкую лодочку, сделанную, например, из фольги, то лодочка будет держаться на поверхности и не «утонет». Этот опыт был показан в передаче «Разрушители легенд» как фокус с «прозрачной водой» (Выпуск 105. Вирусное видео. 7 сезон.)
- Если вдохнуть в себя гексафторид серы, то голос станет низким (действие, противоположное действию гелия).
Примечания
Литература
- Гохберг Б. М. Элегаз — электрическая газовая изоляция (рус.) // «Электричество». — 1947. — № 3. — С. 15.
См. также
dic.academic.ru
Серы гексафторид Википедия
| Фторид серы | |
|---|---|
 | |
| Общие | |
| Традиционные названия | гексафторид серы, шестифтористая сера, элегаз |
| Хим. формула | SF6 |
| Физические свойства | |
| Состояние | газ |
| Молярная масса | 146,06 г/моль |
| Плотность | Газ: 6,164 г/л Жидкость: 1,33 г/см³ |
| Энергия ионизации | 19,3 ± 0,1 эВ[1] |
| Термические свойства | |
| Т. плав. | −50,8 °C |
| −83 ± 1 градус Фаренгейта[1] | |
| Т. кип. | сублимация при −63,9 °C |
| Мол. теплоёмк. | 97,15 Дж/(моль·К) |
| Теплопроводность | 0,012058 Вт/(м·K) |
| Энтальпия образования | −1219 кДж/моль |
| Давление пара | 21,5 ± 0,1 атм[1] |
| Структура | |
| Координационная геометрия | октаэдрическая |
| Кристаллическая структура | орторомбическая |
| Дипольный момент | 0 Д |
| Классификация | |
| Рег. номер CAS | 2551-62-4 |
| PubChem | 17358 |
| Рег. номер EINECS | 219-854-2 |
| SMILES | |
| InChI | |
| RTECS | WS4900000 |
| ChEBI | 30496 |
| Номер ООН | 1080 |
| ChemSpider | 16425 |
| Безопасность | |
| Токсичность | малотоксичен |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Гексафторид серы (также элегаз или шестифтористая сера, SF6) — неорганическое вещество, при стандартных условиях представляет собой тяжёлый газ (в 5 раз тяжелее воздуха). Соединение было впервые получено и описано в 1900 году Анри Муассаном в ходе работ по изучению химии фтора.
Методы получения
Возможно получать гексафторид серы из простых веществ:
- S+3F2→SF6{\displaystyle {\mathsf {S+3F_{2}\rightarrow SF_{6}}}}
Также гексафторид серы образуется при разложении сложных фторидов серы:
- S2F10→SF6+SF4{\displaystyle {\mathsf {S_{2}F_{10}\rightarrow SF_{6}+SF_{4}}}}
Физико-химические свойства
Практически бесцветный газ, без запаха и вкуса. Обладает высоким пробивным напряжением (89 кВ/см — примерно в 3 раза выше, чем у воздуха при нормальном давлении).
Плохо растворим в воде (1 объём SF6 в 200 объёмах воды), этаноле и диэтиловом эфире[2], хорошо растворим в нитрометане.
Плотность элегаза при температуре 273 K и давлении 0,1 МПа составляет 6,56 кг/м³. Относительная диэлектрическая проницаемость — 1,0021. Полное число степеней свободы молекулы элегаза равно 21, из них три степени свободы — в поступательном движении, три — во вращательном, а остальные — в колебательном. Диаметр молекулы равен 5,33 Å.
Термодинамические величины
Химические свойства
Гексафторид серы — достаточно инертное соединение, не реагирует с водой, вероятно, из-за кинетических факторов. Не реагирует также с растворами HCl и NaOH[4], однако при действии восстановителей могут протекать некоторые реакции.
В составе молекулы газа 21,95 % серы и 78,05 % фтора по массе.
Взаимодействие с металлическим натрием проходит только при нагревании, однако уже при 64 °C взаимодействует с раствором натрия в аммиаке:
- SF6+8Na→Na2S+6NaF{\displaystyle {\mathsf {SF_{6}+8Na\rightarrow Na_{2}S+6NaF}}}
Гексафторид серы реагирует с литием с выделением большого количества тепла:
- SF6+6Li→S+6LiF{\displaystyle {\mathsf {SF_{6}+6Li\rightarrow S+6LiF}}}
При этом продукты реакции — элементарная сера и фторид лития — имеют меньший объём, чем исходные вещества, что нашло применение в некоторых экзотических тепловых двигателях (см. ниже).
С водородом и кислородом гексафторид не реагирует. Однако, при сильном нагревании (до 400 °C) SF6 взаимодействует с сероводородом, а при 30 °C — с иодоводородом:
- 2SF6+6h3S→S8+12HF{\displaystyle {\mathsf {2SF_{6}+6H_{2}S\rightarrow S_{8}+12HF}}}
- SF6+8HI→6HF+h3S+4I2{\displaystyle {\mathsf {SF_{6}+8HI\rightarrow 6HF+H_{2}S+4I_{2}}}}
При повышенном давлении и температуре около 500 °C SF6 окисляет PF3 до PF5:
- SF6+PF3→PF5+SF4{\displaystyle {\mathsf {SF_{6}+PF_{3}\rightarrow PF_{5}+SF_{4}}}}
Применение
- как изолятор и теплоноситель в высоковольтной электротехнике;
- как технологическая среда в электронной и металлургической промышленности;
- в системах газового пожаротушения в качестве пожаротушащего вещества;
- как хладагент благодаря высокой теплоёмкости, низкой теплопроводности и низкой вязкости[5];
- для улучшения звукоизоляции в стеклопакетах;
- в полупроводниковой промышленности для плазмохимического травления кремния;
- как окислитель в некоторых экзотических тепловых двигателях — например, в паротурбинной установке американской малогабаритной 324-мм противолодочной торпеды Mark 50, где он используется для окисления металлического лития.
При вдыхании наблюдается эффект пониженной тональности голоса, противоположный действию гелия[6].
Применение в электротехнике
Название «элегаз» шестифтористая сера получила от сокращения «электрический газ». Уникальные свойства элегаза были открыты в СССР, его применение также началось в Советском Союзе. В 30-х годах известный учёный Б. М. Гохберг в ЛФТИ исследовал электрические свойства ряда газов и обратил внимание на некоторые свойства шестифтористой серы SF6 (элегаза)[7]. Потребность в элегазе появилась в стране в начале 1980-х годов и была связана с разработкой и освоением электрооборудования для передач постоянного тока сверхвысокого напряжения. Его промышленное производство в РФ было освоено в 1998 году на Кирово-Чепецком химическом комбинате[8].
Электрическая прочность при атмосферном давлении и зазоре 1 см составляет 89 кВ/см. Характерным является очень большой коэффициент теплового расширения и высокая плотность. Это важно для энергетических установок, в которых проводится охлаждение каких-либо частей устройства, так как при большом коэффициенте теплового расширения легко образуется конвективный поток, уносящий тепло[9].
В центре молекулы элегаза расположен атом серы, а на равном расстоянии от него в вершинах правильного октаэдра располагаются шесть атомов фтора. Это определяет высокую эффективность захвата электронов молекулами, их относительно большую длину свободного пробега и слабую реакционную способность. Поэтому элегаз обладает высокой электрической прочностью.
Элегаз безвреден в смеси с воздухом. Однако вследствие нарушения технологии производства элегаза или его разложения в аппарате под действием электрических разрядов (дугового, коронного, частичных), в элегазе могут возникать чрезвычайно активные в химическом отношении и вредные для человека примеси, а также различные твёрдые соединения, оседающие на стенах конструкции. Интенсивность образования таких примесей зависит от наличия в элегазе примесей кислорода и особенно паров воды.
Некоторое количество элегаза в электротехнической аппаратуре также разлагается в процессе нормальной работы. Например, коммутация тока 31,5 кА в выключателе 110 кВ приводит к разложению 5—7 см³ элегаза на 1 кДж выделяемой в дуге энергии.
Стоимость элегаза довольно высока, однако он нашёл достаточно широкое применение в технике, особенно в высоковольтной электротехнике. Он прежде всего используется как диэлектрик, то есть в качестве основной изоляции для комплектных распределительных устройств, высоковольтных измерительных трансформаторов тока и напряжения и др[10]. Также элегаз используется как среда дугогашения в высоковольтных выключателях[11].
Основные преимущества элегаза перед его основным «конкурентом», трансформаторным маслом, это:
- взрыво- и пожаробезопасность;
- снижения массо-габаритных показателей конструкции за счёт уменьшения изоляционных промежутков и улучшенных условий охлаждения токоведущих частей[источник не указан 1910 дней].
Регламентирующие стандарты
IEC
- IEC 60376:2005 — Технические условия на элегаз (SF6) технического сорта для электрического оборудования.
- IEC 60480:2004 — Руководство по проверке и обработке серы шестифтористой (SF6), взятой из электротехнического оборудования, и технические условия на её повторное использование.
EN[en]
- EN 60376:2005 — Технические условия на элегаз (SF6) технического сорта для электрического оборудования.
- EN 60480:2004 — Руководство по проверке и обработке элегаза (SF6), взятого из электротехнического оборудования, и технические условия на его повторное использование.
Вредное воздействие
- Основной источник: [12]
По степени воздействия на организм человека относится к малоопасным веществам (4-й класс согласно ГОСТ 12.1.007-76).
Имеется возможность отравления продуктами распада элегаза (низшими фторидами), образующимися, например, при работе дугогасительных камер в высоковольтных выключателях.
Потенциал разрушения озонового слоя ODP = 0.
Сильнейший известный парниковый газ, потенциал глобального потепления GWP = 24 900. Из-за небольших объёмов изготовления вклад в глобальное потепление не превышает 0,2 %. Регламентируется Киотским протоколом.
Интересные факты
- Если наполнить гексафторидом серы открытый сверху сосуд (так как газ тяжелее воздуха, то он не будет «выливаться» из сосуда) и поместить туда лёгкую лодочку, сделанную, например, из фольги, то лодочка будет держаться на поверхности и не «утонет». Этот опыт был показан в передаче «Разрушители легенд» как фокус с «прозрачной водой»[13]. Так же, из-за высокой плотности, скорость звука в этом газе значительно ниже, чем в воздухе, что приводит к комичному эффекту при вдыхании газа — голос становится очень низким и грубым, подобно голосу Дарта Вейдера. Опыт также демонстрировался в передаче «Разрушители легенд». Аналогичный эффект создаёт и ксенон. А гелий — который в 6 раз легче воздуха — при вдыхании наоборот создаёт тонкий и писклявый голос.
Примечания
- ↑ 1 2 3 http://www.cdc.gov/niosh/npg/npgd0576.html
- ↑ Свойства гексафторида серы на сайте «Химик.ру»
- ↑ 1 2 Sulfur hexafluoride. Air Liquide Gas Encyclopedia. Проверено 22 февраля 2013.
- ↑ Успехи химии, 1975, Том 44, Номер 2, Страницы 193—213.
- ↑ Применение шестифтористой серы
- ↑ Фрагмент передачи «Разрушители мифов»
- ↑ Гохберг Б. М. Ленинградский физико-технический институт Академии наук СССР (рус.) // Успехи физических наук. — 1940. — Т. XXIV, вып. 1. — С. 11-20. См. стр. 16-17, раздел «Электрическая прочность газов»
- ↑ Уткин В. В. Завод у двуречья. Кирово-Чепецкий химический комбинат имени Б. П. Константинова: строительство, развитие, люди. — Киров: ОАО «Дом печати — Вятка», 2007. — Т. 4 (1973—1992), часть 1. — С. 66—67. — 144 с. — 1000 экз. — ISBN 978-5-85271-293-6.
- ↑ Коробейников С.М., д.ф.м.н., профессор. Диэлектрические материалы. 4.1.2. Электроотрицательные газы, применение газообразных диэлектриков. (рус.). Проверено 2 июня 2011. Архивировано 20 февраля 2012 года.
- ↑ ЗВА :: Измерительные трансформаторы с газовой изоляцией
- ↑ Применение SF6 в высоковольтной электронике.
- ↑ Элегаз. Свойства
- ↑ Выпуск 105. Вирусное видео. 6 сезон
Литература
- Гохберг Б. М. Элегаз — электрическая газовая изоляция (рус.) // «Электричество». — 1947. — № 3. — С. 15.
См. также
wikiredia.ru
Гексафторид серы Вики
| Фторид серы | |
|---|---|
 | |
| Общие | |
| Традиционные названия | гексафторид серы, шестифтористая сера, элегаз |
| Хим. формула | SF6 |
| Физические свойства | |
| Состояние | газ |
| Молярная масса | 146,06 г/моль |
| Плотность | Газ: 6,164 г/л Жидкость: 1,33 г/см³ |
| Энергия ионизации | 19,3 ± 0,1 эВ[1] |
| Термические свойства | |
| Т. плав. | −50,8 °C |
| −83 ± 1 градус Фаренгейта[1] | |
| Т. кип. | сублимация при −63,9 °C |
| Мол. теплоёмк. | 97,15 Дж/(моль·К) |
| Теплопроводность | 0,012058 Вт/(м·K) |
| Энтальпия образования | −1219 кДж/моль |
| Давление пара | 21,5 ± 0,1 атм[1] |
| Структура | |
| Координационная геометрия | октаэдрическая |
| Кристаллическая структура | орторомбическая |
| Дипольный момент | 0 Д |
| Классификация | |
| Рег. номер CAS | 2551-62-4 |
| PubChem | 17358 |
| Рег. номер EINECS | 219-854-2 |
| SMILES | |
| InChI | |
| RTECS | WS4900000 |
| ChEBI | 30496 |
| Номер ООН | 1080 |
| ChemSpider | 16425 |
| Безопасность | |
| Токсичность | малотоксичен |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Гексафторид серы (также элегаз или шестифтористая сера, SF6) — неорганическое вещество, при стандартных условиях представляет собой тяжёлый газ (в 5 раз тяжелее воздуха). Соединение было впервые получено и описано в 1900 году Анри Муассаном в ходе работ по изучению химии фтора.
Методы получения[ | код]
Возможно получать гексафторид серы из простых веществ:
- S+3F2→SF6{\displaystyle {\mathsf {S+3F_{2}\rightarrow SF_{6}}}}
Также гексафторид серы образуется при разложении сложных фторидов серы:
- S2F10→SF6+SF4{\displaystyle {\mathsf {S_{2}F_{10}\rightarrow SF_{6}+SF_{4}}}}
Физико-химические свойства[ | код]
Практически бесцветный газ, без запаха и вкуса. Обладает высоким пробивным напряжением (89 кВ/см — примерно в 3 раза выше, чем у воздуха при нормальном давлении).
Плохо растворим в воде (1 объём SF6 в 200 объёмах воды), этаноле и диэтиловом эфире[2], хорошо растворим в нитрометане.
Плотность элегаза при температуре 273 K и давлении 0,1 МПа составляет 6,56 кг/м³. Относительная диэлектрическая проницаемость — 1,0021. Полное число степеней свободы молекулы элегаза равно 21, из них три степени свободы — в поступательном движении, три — во вращательном, а остальные — в колебательном. Диаметр молекулы равен 5,33 Å.
Термодинамические величины[ | код]
Химические свойства[ | код]
Гексафторид серы — достаточно инертное соединение, не реагирует с водой, вероятно, из-за кинетических факторов. Не реагирует также с растворами HCl и NaOH[4], однако при действии восстановителей могут протекать некоторые реакции.
В составе молекулы газа 21,95 % серы и 78,05 % фтора по массе.
Взаимодействие с металлическим натрием проходит только при нагревании, однако уже при 64 °C взаимодействует с раствором натрия в аммиаке:
- SF6+8Na→Na2S+6NaF{\displaystyle {\mathsf {SF_{6}+8Na\rightarrow Na_{2}S+6NaF}}}
Гексафторид серы реагирует с литием с выделением большого количества тепла:
- SF6+6Li→S+6LiF{\displaystyle {\mathsf {SF_{6}+6Li\rightarrow S+6LiF}}}
При этом продукты реакции — элементарная сера и фторид лития — имеют меньший объём, чем исходные вещества, что нашло применение в некоторых экзотических тепловых двигателях (см. ниже).
С водородом и кислородом гексафторид не реагирует. Однако, при сильном нагревании (до 400 °C) SF6 взаимодействует с сероводородом, а при 30 °C — с иодоводородом:
- 2SF6+6h3S→S8+12HF{\displaystyle {\mathsf {2SF_{6}+6H_{2}S\rightarrow S_{8}+12HF}}}
- SF6+8HI→6HF+h3S+4I2{\displaystyle {\mathsf {SF_{6}+8HI\rightarrow 6HF+H_{2}S+4I_{2}}}}
При повышенном давлении и температуре около 500 °C SF6 окисляет PF3 до PF5:
- SF6+PF3→PF5+SF4{\displaystyle {\mathsf {SF_{6}+PF_{3}\rightarrow PF_{5}+SF_{4}}}}
Применение[ | код]
- как изолятор и теплоноситель в высоковольтной электротехнике;
- как технологическая среда в электронной и металлургической промышленности;
- в системах газового пожаротушения в качестве пожаротушащего вещества;
- как хладагент благодаря высокой теплоёмкости, низкой теплопроводности и низкой вязкости[5];
- для улучшения звукоизоляции в стеклопакетах;
- в полупроводниковой промышленности для плазмохимического травления кремния;
- как окислитель в некоторых экзотических тепловых двигателях — например, в паротурбинной установке американской малогабаритной 324-мм противолодочной торпеды Mark 50, где он используется для окисления металлического лития.
При вдыхании наблюдается эффект пониженной тональности голоса, противоположный действию гелия[6].
Применение в электротехнике[ | код]
Название «элегаз» шестифтористая сера получила от сокращения «электрический газ». Уникальные свойства элегаза были открыты в СССР, его применение также началось в Советском Союзе. В 30-х годах известный учёный Б. М. Гохберг в ЛФТИ исследовал электрические свойства ряда газов и обратил внимание на некоторые свойства шестифтористой серы SF6 (элегаза)[7]. Потребность в элегазе появилась в стране в начале 1980-х годов и была связана с разработкой и освоением электрооборудования для передач постоянного тока сверхвысокого напряжения. Его промышленное производство в РФ было освоено в 1998 году на Кирово-Чепецком химическом комбинате[8].
Электрическая прочность при атмосферном давлении и зазоре 1 см составляет 89 кВ/см. Характерным является очень большой коэффициент теплового расширения и высокая плотность. Это важно для энергетических установок, в которых проводится охлаждение каких-либо частей устройства, так как при большом коэффициенте теплового расширения легко образуется конвективный поток, уносящий тепло[9].
В центре молекулы элегаза расположен атом серы, а на равном расстоянии от него в вершинах правильного октаэдра располагаются шесть атомов фтора. Это определяет высокую эффективность захвата электронов молекулами, их относительно большую длину свободного пробега и слабую реакционную способность. Поэтому элегаз обладает высокой электрической прочностью.
Элегаз безвреден в смеси с воздухом. Однако вследствие нарушения технологии производства элегаза или его разложения в аппарате под действием электрических разрядов (дугового, коронного, частичных), в элегазе могут возникать чрезвычайно активные в химическом отношении и вредные для человека примеси, а также различные твёрдые соединения, оседающие на стенах конструкции. Интенсивность образования таких примесей зависит от наличия в элегазе примесей кислорода и особенно паров воды.
Некоторое количество элегаза в электротехнической аппаратуре также разлагается в процессе нормальной работы. Например, коммутация тока 31,5 кА в выключателе 110 кВ приводит к разложению 5—7 см³ элегаза на 1 кДж выделяемой в дуге энергии.
Стоимость элегаза довольно высока, однако он нашёл достаточно широкое применение в технике, особенно в высоковольтной электротехнике. Он прежде всего используется как диэлектрик, то есть в качестве основной изоляции для комплектных распределительных устройств, высоковольтных измерительных трансформаторов тока и напряжения и др[10]. Также элегаз используется как среда дугогашения в высоковольтных выключателях[11].
Основные преимущества элегаза перед его основным «конкурентом», трансформаторным маслом, это:
- взрыво- и пожаробезопасность;
- снижения массо-габаритных показателей конструкции за счёт уменьшения изоляционных промежутков и улучшенных условий охлаждения токоведущих частей[источник не указан 1910 дней].
Регламентирующие стандарты[ | код]
IEC
- IEC 60376:2005 — Технические условия на элегаз (SF6) технического сорта для электрического оборудования.
- IEC 60480:2004 — Руководство по проверке и обработке серы шестифтористой (SF6), взятой из электротехнического оборудования, и технические условия на её повторное использование.
EN[en]
- EN 60376:2005 — Технические условия на элегаз (SF6) технического сорта для электрического оборудования.
- EN 60480:2004 — Руководство по проверке и обработке элегаза (SF6), взятого из электротехнического оборудования, и технические условия на его повторное использование.
Вредное воздействие[ | код]
- Основной источник: [12]
По степени воздействия на организм человека относится к малоопасным веществам (4-й класс согласно ГОСТ 12.1.007-76).
Имеется возможность отравления продуктами распада элегаза (низшими фторидами), образующимися, например, при работе дугогасительных камер в высоковольтных выключателях.
Потенциал разрушения озонового слоя ODP = 0.
Сильнейший известный парниковый газ, потенциал глобального потепления GWP = 24 900. Из-за небольших объёмов изготовления вклад в глобальное потепление не превышает 0,2 %. Регламентируется Киотским протоколом.
Интересные факты[ | код]
- Если наполнить гексафторидом серы открытый сверху сосуд (так как газ тяжелее воздуха, то он не будет «выливаться» из сосуда) и поместить туда лёгкую лодочку, сделанную, например, из фольги, то лодочка будет держаться на поверхности и не «утонет». Этот опыт был показан в передаче «Разрушители легенд» как фокус с «прозрачной водой»[13]. Так же, из-за высокой плотности, скорость звука в этом газе значительно ниже, чем в воздухе, что приводит к комичному эффекту при вдыхании газа — голос становится очень низким и грубым, подобно голосу Дарта Вейдера. Опыт также демонстрировался в передаче «Разрушители легенд». Аналогичный эффект создаёт и ксенон. А гелий — который в 6 раз легче воздуха — при вдыхании наоборот создаёт тонкий и писклявый голос.
Примечания[ | код]
- ↑ 1 2 3 http://www.cdc.gov/niosh/npg/npgd0576.html
- ↑ Свойства гексафторида серы на сайте «Химик.ру»
- ↑ 1 2 Sulfur hexafluoride. Air Liquide Gas Encyclopedia. Проверено 22 февраля 2013.
- ↑ Успехи химии, 1975, Том 44, Номер 2, Страницы 193—213.
- ↑ Применение шестифтористой серы
- ↑ Фрагмент передачи «Разрушители мифов»
- ↑ Гохберг Б. М. Ленинградский физико-технический институт Академии наук СССР (рус.) // Успехи физических наук. — 1940. — Т. XXIV, вып. 1. — С. 11-20. См. стр. 16-17, раздел «Электрическая прочность газов»
- ↑ Уткин В. В. Завод у двуречья. Кирово-Чепецкий химический комбинат имени Б. П. Константинова: строительство, развитие, люди. — Киров: ОАО «Дом печати — Вятка», 2007. — Т. 4 (1973—1992), часть 1. — С. 66—67. — 144 с. — 1000 экз. — ISBN 978-5-85271-293-6.
- ↑ Коробейников С.М., д.ф.м.н., профессор. Диэлектрические материалы. 4.1.2. Электроотрицательные газы, применение газообразных диэлектриков. (рус.). Проверено 2 июня 2011. Архивировано 20 февраля 2012 года.
- ↑ ЗВА :: Измерительные трансформаторы с газовой изоляцией
- ↑ Применение SF6 в высоковольтной электронике.
- ↑ Элегаз. Свойства
- ↑ Выпуск 105. Вирусное видео. 6 сезон
Литература[ | код]
- Гохберг Б. М. Элегаз — электрическая газовая изоляция (рус.) // «Электричество». — 1947. — № 3. — С. 15.
См. также[ | код]
ru.wikibedia.ru
| Фторид серы | |
|---|---|
 | |
| Общие | |
| Традиционные названия | гексафторид серы, шестифтористая сера, элегаз |
| Хим. формула | SF6 |
| Физические свойства | |
| Состояние | газ |
| Молярная масса | 146,06 г/моль |
| Плотность | Газ: 6,164 г/л Жидкость: 1,33 г/см³ |
| Энергия ионизации | 19,3 ± 0,1 эВ[1] |
| Термические свойства | |
| Т. плав. | −50,8 °C |
| −83 ± 1 градус Фаренгейта[1] | |
| Т. кип. | сублимация при −63,9 °C |
| Мол. теплоёмк. | 97,15 Дж/(моль·К) |
| Теплопроводность | 0,012058 Вт/(м·K) |
| Энтальпия образования | −1219 кДж/моль |
| Давление пара | 21,5 ± 0,1 атм[1] |
| Структура | |
| Координационная геометрия | октаэдрическая |
| Кристаллическая структура | орторомбическая |
| Дипольный момент | 0 Д |
| Классификация | |
| Рег. номер CAS | 2551-62-4 |
| PubChem | 17358 |
| Рег. номер EINECS | 219-854-2 |
| SMILES | |
| InChI | |
| RTECS | WS4900000 |
| ChEBI | 30496 |
| Номер ООН | 1080 |
| ChemSpider | 16425 |
| Безопасность | |
| Токсичность | |
ru-wiki.ru
Серы гексафторид Вики
| Фторид серы | |
|---|---|
 | |
| Общие | |
| Традиционные названия | гексафторид серы, шестифтористая сера, элегаз |
| Хим. формула | SF6 |
| Физические свойства | |
| Состояние | газ |
| Молярная масса | 146,06 г/моль |
| Плотность | Газ: 6,164 г/л Жидкость: 1,33 г/см³ |
| Энергия ионизации | 19,3 ± 0,1 эВ[1] |
| Термические свойства | |
| Т. плав. | −50,8 °C |
| −83 ± 1 градус Фаренгейта[1] | |
| Т. кип. | сублимация при −63,9 °C |
| Мол. теплоёмк. | 97,15 Дж/(моль·К) |
| Теплопроводность | 0,012058 Вт/(м·K) |
| Энтальпия образования | −1219 кДж/моль |
| Давление пара | 21,5 ± 0,1 атм[1] |
| Структура | |
| Координационная геометрия | октаэдрическая |
| Кристаллическая структура | орторомбическая |
| Дипольный момент | 0 Д |
| Классификация | |
| Рег. номер CAS | 2551-62-4 |
| PubChem | 17358 |
| Рег. номер EINECS | 219-854-2 |
| SMILES | |
| InChI | |
| RTECS | WS4900000 |
| ChEBI | 30496 |
| Номер ООН | 1080 |
| ChemSpider | 16425 |
| Безопасность | |
| Токсичность | малотоксичен |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Гексафторид серы (также элегаз или шестифтористая сера, SF6) — неорганическое вещество, при стандартных условиях представляет собой тяжёлый газ (в 5 раз тяжелее воздуха). Соединение было впервые получено и описано в 1900 году Анри Муассаном в ходе работ по изучению химии фтора.
Методы получения[ | код]
Возможно получать гексафторид серы из простых веществ:
- S+3F2→SF6{\displaystyle {\mathsf {S+3F_{2}\rightarrow SF_{6}}}}
Также гексафторид серы образуется при разложении сложных фторидов серы:
- S2F10→SF6+SF4{\displaystyle {\mathsf {S_{2}F_{10}\rightarrow SF_{6}+SF_{4}}}}
Физико-химические свойства[ | код]
Практически бесцветный газ, без запаха и вкуса. Обладает высоким пробивным напряжением (89 кВ/см — примерно в 3 раза выше, чем у воздуха при нормальном давлении).
Плохо растворим в воде (1 объём SF6 в 200 объёмах воды), этаноле и диэтиловом эфире[2], хорошо растворим в нитрометане.
Плотность элегаза при температуре 273 K и давлении 0,1 МПа составляет 6,56 кг/м³. Относительная диэлектрическая проницаемость — 1,0021. Полное число степеней свободы молекулы элегаза равно 21, из них три степени свободы — в поступательном движении, три — во вращательном, а остальные — в колебательном. Диаметр молекулы равен 5,33 Å.
Термодинамические величины[ | код]
Химические свойства[ | код]
Гексафторид серы — достаточно инертное соединение, не реагирует с водой, вероятно, из-за кинетических факторов. Не реагирует также с растворами HCl и NaOH[4], однако при действии восстановителей могут протекать некоторые реакции.
В составе молекулы газа 21,95 % серы и 78,05 % фтора по массе.
Взаимодействие с металлическим натрием проходит только при нагревании, однако уже при 64 °C взаимодействует с раствором натрия в аммиаке:
- SF6+8Na→Na2S+6NaF{\displaystyle {\mathsf {SF_{6}+8Na\rightarrow Na_{2}S+6NaF}}}
Гексафторид серы реагирует с литием с выделением большого количества тепла:
- SF6+6Li→S+6LiF{\displaystyle {\mathsf {SF_{6}+6Li\rightarrow S+6LiF}}}
При этом продукты реакции — элементарная сера и фторид лития — имеют меньший объём, чем исходные вещества, что нашло применение в некоторых экзотических тепловых двигателях (см. ниже).
С водородом и кислородом гексафторид не реагирует. Однако, при сильном нагревании (до 400 °C) SF6 взаимодействует с сероводородом, а при 30 °C — с иодоводородом:
- 2SF6+6h3S→S8+12HF{\displaystyle {\mathsf {2SF_{6}+6H_{2}S\rightarrow S_{8}+12HF}}}
- SF6+8HI→6HF+h3S+4I2{\displaystyle {\mathsf {SF_{6}+8HI\rightarrow 6HF+H_{2}S+4I_{2}}}}
При повышенном давлении и температуре около 500 °C SF6 окисляет PF3 до PF5:
- SF6+PF3→PF5+SF4{\displaystyle {\mathsf {SF_{6}+PF_{3}\rightarrow PF_{5}+SF_{4}}}}
Применение[ | код]
- как изолятор и теплоноситель в высоковольтной электротехнике;
- как технологическая среда в электронной и металлургической промышленности;
- в системах газового пожаротушения в качестве пожаротушащего вещества;
- как хладагент благодаря высокой теплоёмкости, низкой теплопроводности и низкой вязкости[5];
- для улучшения звукоизоляции в стеклопакетах;
- в полупроводниковой промышленности для плазмохимического травления кремния;
- как окислитель в некоторых экзотических тепловых двигателях — например, в паротурбинной установке американской малогабаритной 324-мм противолодочной торпеды Mark 50, где он используется для окисления металлического лития.
При вдыхании наблюдается эффект пониженной тональности голоса, противоположный действию гелия[6].
Применение в электротехнике[ | код]
Название «элегаз» шестифтористая сера получила от сокращения «электрический газ». Уникальные свойства элегаза были открыты в СССР, его применение также началось в Советском Союзе. В 30-х годах известный учёный Б. М. Гохберг в ЛФТИ исследовал электрические свойства ряда газов и обратил внимание на некоторые свойства шестифтористой серы SF6 (элегаза)[7]. Потребность в элегазе появилась в стране в начале 1980-х годов и была связана с разработкой и освоением электрооборудования для передач постоянного тока сверхвысокого напряжения. Его промышленное производство в РФ было освоено в 1998 году на Кирово-Чепецком химическом комбинате[8].
Электрическая прочность при атмосферном давлении и зазоре 1 см составляет 89 кВ/см. Характерным является очень большой коэффициент теплового расширения и высокая плотность. Это важно для энергетических установок, в которых проводится охлаждение каких-либо частей устройства, так как при большом коэффициенте теплового расширения легко образуется конвективный поток, уносящий тепло[9].
В центре молекулы элегаза расположен атом серы, а на равном расстоянии от него в вершинах правильного октаэдра располагаются шесть атомов фтора. Это определяет высокую эффективность захвата электронов молекулами, их относительно большую длину свободного пробега и слабую реакционную способность. Поэтому элегаз обладает высокой электрической прочностью.
Элегаз безвреден в смеси с воздухом. Однако вследствие нарушения технологии производства элегаза или его разложения в аппарате под действием электрических разрядов (дугового, коронного, частичных), в элегазе могут возникать чрезвычайно активные в химическом отношении и вредные для человека примеси, а также различные твёрдые соединения, оседающие на стенах конструкции. Интенсивность образования таких примесей зависит от наличия в элегазе примесей кислорода и особенно паров воды.
Некоторое количество элегаза в электротехнической аппаратуре также разлагается в процессе нормальной работы. Например, коммутация тока 31,5 кА в выключателе 110 кВ приводит к разложению 5—7 см³ элегаза на 1 кДж выделяемой в дуге энергии.
Стоимость элегаза довольно высока, однако он нашёл достаточно широкое применение в технике, особенно в высоковольтной электротехнике. Он прежде всего используется как диэлектрик, то есть в качестве основной изоляции для комплектных распределительных устройств, высоковольтных измерительных трансформаторов тока и напряжения и др[10]. Также элегаз используется как среда дугогашения в высоковольтных выключателях[11].
Основные преимущества элегаза перед его основным «конкурентом», трансформаторным маслом, это:
- взрыво- и пожаробезопасность;
- снижения массо-габаритных показателей конструкции за счёт уменьшения изоляционных промежутков и улучшенных условий охлаждения токоведущих частей[источник не указан 1910 дней].
Регламентирующие стандарты[ | код]
IEC
- IEC 60376:2005 — Технические условия на элегаз (SF6) технического сорта для электрического оборудования.
- IEC 60480:2004 — Руководство по проверке и обработке серы шестифтористой (SF6), взятой из электротехнического оборудования, и технические условия на её повторное использование.
EN[en]
- EN 60376:2005 — Технические условия на элегаз (SF6) технического сорта для электрического оборудования.
- EN 60480:2004 — Руководство по проверке и обработке элегаза (SF6), взятого из электротехнического оборудования, и технические условия на его повторное использование.
Вредное воздействие[ | код]
- Основной источник: [12]
По степени воздействия на организм человека относится к малоопасным веществам (4-й класс согласно ГОСТ 12.1.007-76).
Имеется возможность отравления продуктами распада элегаза (низшими фторидами), образующимися, например, при работе дугогасительных камер в высоковольтных выключателях.
Потенциал разрушения озонового слоя ODP = 0.
Сильнейший известный парниковый газ, потенциал глобального потепления GWP = 24 900. Из-за небольших объёмов изготовления вклад в глобальное потепление не превышает 0,2 %. Регламентируется Киотским протоколом.
Интересные факты[ | код]
- Если наполнить гексафторидом серы открытый сверху сосуд (так как газ тяжелее воздуха, то он не будет «выливаться» из сосуда) и поместить туда лёгкую лодочку, сделанную, например, из фольги, то лодочка будет держаться на поверхности и не «утонет». Этот опыт был показан в передаче «Разрушители легенд» как фокус с «прозрачной водой»[13]. Так же, из-за высокой плотности, скорость звука в этом газе значительно ниже, чем в воздухе, что приводит к комичному эффекту при вдыхании газа — голос становится очень низким и грубым, подобно голосу Дарта Вейдера. Опыт также демонстрировался в передаче «Разрушители легенд». Аналогичный эффект создаёт и ксенон. А гелий — который в 6 раз легче воздуха — при вдыхании наоборот создаёт тонкий и писклявый голос.
Примечания[ | код]
- ↑ 1 2 3 http://www.cdc.gov/niosh/npg/npgd0576.html
- ↑ Свойства гексафторида серы на сайте «Химик.ру»
- ↑ 1 2 Sulfur hexafluoride. Air Liquide Gas Encyclopedia. Проверено 22 февраля 2013.
- ↑ Успехи химии, 1975, Том 44, Номер 2, Страницы 193—213.
- ↑ Применение шестифтористой серы
- ↑ Фрагмент передачи «Разрушители мифов»
- ↑ Гохберг Б. М. Ленинградский физико-технический институт Академии наук СССР (рус.) // Успехи физических наук. — 1940. — Т. XXIV, вып. 1. — С. 11-20. См. стр. 16-17, раздел «Электрическая прочность газов»
- ↑ Уткин В. В. Завод у двуречья. Кирово-Чепецкий химический комбинат имени Б. П. Константинова: строительство, развитие, люди. — Киров: ОАО «Дом печати — Вятка», 2007. — Т. 4 (1973—1992), часть 1. — С. 66—67. — 144 с. — 1000 экз. — ISBN 978-5-85271-293-6.
- ↑ Коробейников С.М., д.ф.м.н., профессор. Диэлектрические материалы. 4.1.2. Электроотрицательные газы, применение газообразных диэлектриков. (рус.). Проверено 2 июня 2011. Архивировано 20 февраля 2012 года.
- ↑ ЗВА :: Измерительные трансформаторы с газовой изоляцией
- ↑ Применение SF6 в высоковольтной электронике.
- ↑ Элегаз. Свойства
- ↑ Выпуск 105. Вирусное видео. 6 сезон
Литература[ | код]
- Гохберг Б. М. Элегаз — электрическая газовая изоляция (рус.) // «Электричество». — 1947. — № 3. — С. 15.
См. также[ | код]
ru.wikibedia.ru